เซลล์ไฟฟ้าเคมีแบบกัลวานิกเครื่องแรกของโลกได้รับการพัฒนาโดยลุยจิ กัลวานี อ่านเกี่ยวกับประวัติความเป็นมาได้ที่นี่ ในบทความนี้โดยพื้นฐานแล้ว มันคือแหล่งจ่ายกระแสไฟฟ้าชั่วคราวที่เกิดจากปฏิกิริยาเคมี การไหลของอิเล็กตรอนเกิดขึ้นจากการปฏิสัมพันธ์ระหว่างโลหะสองชนิดที่แตกต่างกัน ผลที่ได้คือ พลังงานเคมีถูกแปลงเป็นพลังงานไฟฟ้า ซึ่งสามารถนำไปใช้ในชีวิตประจำวันได้
เซลล์กัลวานิกแบบความเข้มข้นเป็นแหล่งกำเนิดกระแสไฟฟ้าที่ประกอบด้วยขั้วไฟฟ้าโลหะสองขั้วที่เหมือนกัน วางอยู่ในส่วนผสมของเกลือของโลหะชนิดนั้นในความเข้มข้นต่างๆ กัน
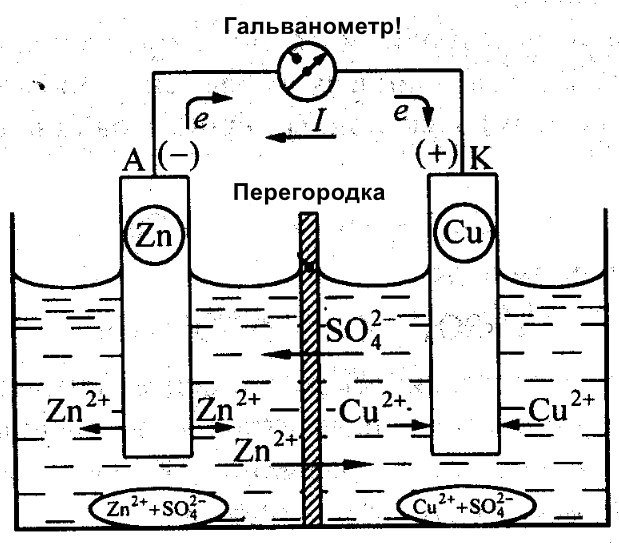
นอกจากกัลวานีแล้ว แดเนียล จาโคบีก็ทำงานเกี่ยวกับการสร้างแบตเตอรี่ที่มีประสิทธิภาพเช่นกัน เขาได้ปรับเปลี่ยนแหล่งพลังงานของเขาเล็กน้อย โดยประกอบด้วยแผ่นทองแดงที่วางอยู่ใน CuSO4 และแผ่นสังกะสีที่จุ่มอยู่ใน ZnSO4 เพื่อป้องกันไม่ให้สารทั้งสองทำปฏิกิริยากันโดยตรง จึงมีการวางผนังพรุนไว้ระหว่างกัน ด้านล่างนี้คือแผนภาพของเซลล์กัลวานิกของแดเนียล จาโคบี
สังกะสีและทองแดงมีปฏิกิริยาทางเคมีที่แตกต่างกัน ดังนั้นประจุของพวกมันจึงแตกต่างกัน ส่งผลให้ระดับประจุของขั้วไฟฟ้าไม่สม่ำเสมอ ทำให้พวกมันเคลื่อนที่และสร้างกระแสไฟฟ้าหรือกระแสกัลวานิกได้ กระแสไฟฟ้านี้จะเริ่มไหลเมื่อบุคคลหรือผู้ประดิษฐ์อุปกรณ์เก็บกระแสไฟฟ้าเชื่อมต่อโหลด โหลดนั้นอาจเป็นหลอดไฟ วิทยุ เมาส์คอมพิวเตอร์ หรืออุปกรณ์ไฟฟ้าอื่นๆ
แผนภาพแสดงวงจรของเซลล์กัลวานิก
แผนภาพวงจรหมายถึงองค์ประกอบและโครงสร้างของมัน วงจรสามารถสร้างขึ้นจากธาตุเคมีหลายชนิดโดยใช้อุปกรณ์เสริม ด้านล่างนี้จะอธิบายโครงสร้างของเซลล์กัลวานิกโดยสังเขป อ่านเพิ่มเติมได้ในบทความนี้!
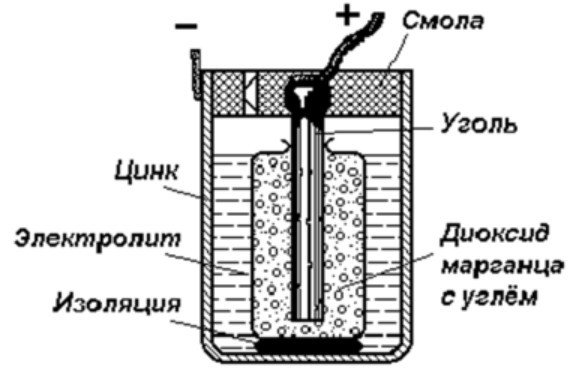
โครงสร้างของเซลล์กัลวานิก
อุปกรณ์กักเก็บพลังงานที่ง่ายที่สุดประกอบด้วย:
- แท่งถ่านหิน
- โลหะสองชนิดที่แตกต่างกัน
- อิเล็กโทรไลต์
- เรซินหรือพลาสติก
- ฉนวน.
จากแผนภาพนี้ จะเห็นได้ว่าเซลล์กัลวานิกประกอบด้วยขั้วลบและขั้วบวก เซลล์เหล่านี้สามารถทำจากทองแดง สังกะสี หรือโลหะอื่นๆ บางครั้งก็เรียกว่าเซลล์ทองแดง-สังกะสี หรือเรียกอีกอย่างว่า... แบตเตอรี่แห้ง.
การกำหนดตำแหน่งเซลล์กัลวานิกในแผนภาพ มันถูกสร้างขึ้นในรูปทรงของเส้นแนวตั้งสองเส้นที่อยู่ใกล้กันในระยะห่างเล็กน้อย โดยเส้นหนึ่งจะเล็กกว่า ที่ขอบของแต่ละเส้นจะมีสัญลักษณ์บ่งบอก ขั้วเส้นยาวแสดงถึงขั้วบวก และเส้นสั้นแสดงถึงขั้วลบ อาจมีการระบุแรงดันไฟฟ้าไว้ข้างๆ ด้วย ซึ่งหมายความว่าวงจรที่ใช้แบตเตอรี่จะทำงานได้เฉพาะที่แรงดันไฟฟ้านั้นเท่านั้น
หลักการทำงานของเซลล์ไฟฟ้าเคมี
เซลล์กัลวานิกทำงานโดยอาศัยการเคลื่อนที่ของอิเล็กตรอนจากขั้วโลหะหนึ่งไปยังอีกขั้วหนึ่ง ทำให้เกิดการเปลี่ยนแปลงทางเคมี อ่านเพิ่มเติมเกี่ยวกับอุณหพลศาสตร์ของเซลล์กัลวานิกและการเกิดกระแสไฟฟ้ากัลวานิก ที่นี่.
คำตอบสำหรับคำถามที่พบบ่อย
| กัลวานิก | คำอธิบาย |
| แบตเตอรี่ | แหล่งพลังงานที่ทำงานผ่านกระบวนการที่เกิดขึ้นภายในพื้นที่จำกัดขนาดเล็ก โดยเฉพาะอย่างยิ่ง พลังงานจะถูกสร้างขึ้นผ่านปฏิกิริยาเคมี |
| เซลล์ไฟฟ้าเคมี หรือ กองเซลล์ไฟฟ้าเคมี | นี่คือธาตุพลังงานที่นักวิทยาศาสตร์ชื่อโวลต์คิดค้นขึ้นเป็นครั้งแรก |
| กระบวนการ | ปฏิกิริยาระหว่างธาตุทางเคมีที่ส่งผลให้เกิดกระแสไฟฟ้า |
| การจำหน่าย | นี่คือจุดสิ้นสุดของปฏิกิริยาเคมี กล่าวคือ จะไม่มีปฏิกิริยาระหว่างสารต่างๆ อีกต่อไป การปล่อยประจุไฟฟ้า (Galvanic discharge) มีอยู่ในเกม Warframe โดยพื้นฐานแล้วมันคือการดัดแปลงที่หายาก ใช้สำหรับอาวุธระยะประชิด ขั้วเวอร์ชัน 2 |
| การสัมผัสทางไฟฟ้า | นี่คือจุดสัมผัสระหว่างขั้วไฟฟ้ากับสารละลาย |
| ผล | การปรากฏของความแตกต่างระหว่างหน้าสัมผัสสองจุดที่ทำจากโลหะสองชนิด ขนาดของความแตกต่างขึ้นอยู่กับอุณหภูมิและองค์ประกอบทางเคมีของตัวนำ โดยพื้นฐานแล้วนี่คือกฎข้อแรกของโวลตา |
| การเชื่อมต่อ/การเชื่อมโยง/ห่วงโซ่ | การเชื่อมต่อส่วนต่างๆ ของวงจรไฟฟ้าตั้งแต่สองส่วนขึ้นไปเข้ากับแหล่งจ่ายกระแสไฟฟ้า |
| ประจุไฟฟ้า | เติมพลังงานให้กับแบตเตอรี่ |
การชุบสังกะสีเป็นกระบวนการทางเคมีโดยใช้กระแสไฟฟ้า ปฏิกิริยาจะลดปริมาณไอออนโลหะที่ละลายลงจนกระทั่งในที่สุดไอออนเหล่านั้นจะก่อตัวเป็นชั้นเคลือบที่สม่ำเสมอบนขั้วโลหะ ส่งผลให้ชิ้นงานมีความทนทานมากขึ้น รอยบุบเล็กๆ หายไป และมีรูปลักษณ์ที่สวยงามยิ่งขึ้น
ประเภทของเซลล์กัลวานิก
แบตเตอรี่มีหลายประเภทเฉพาะเจาะจง
ตารางเซลล์ไฟฟ้าเคมี
| พิมพ์ | แรงดันไฟฟ้า | ข้อได้เปรียบหลัก |
| ลิเธียม | 3 โวลต์ | ใหญ่ ความจุกระแสไฟฟ้าสูง |
| แบตเตอรี่เกลือ หรือคาร์บอน-สังกะสี | 1.5 นิ้ว | ราคาถูกที่สุด |
| นิกเกิลออกซีไฮดรอกซิล NiOOH | 1.6 โวลต์ | กระแสไฟฟ้าสูง ความจุสูง |
| ด่างหรืออัลคาไลน์ | 1.6 โวลต์ | กระแสไฟสูง เสียงดังฟังชัด |
หัวข้อนี้จะกล่าวถึงโดยละเอียดในบทความ ประเภทของแบตเตอรี่!
วัตถุประสงค์ของเซลล์กัลวานิก
อุปกรณ์นี้ออกแบบมาเพื่อใช้ในการสตาร์ทอุปกรณ์ไฟฟ้า ซึ่งอาจรวมถึง:
- ดู.
- รีโมทคอนโทรล
- ไฟฉาย
- อุปกรณ์ทางการแพทย์
- แล็ปท็อป
- ของเล่น
- พวงกุญแจ
- โทรศัพท์
- เลเซอร์พอยเตอร์
- เครื่องคิดเลข
และสิ่งต่างๆ ที่คล้ายคลึงกันรอบตัวเรา
เซลล์ไฟฟ้าเคมีที่บ้าน
คุณสามารถสร้างแหล่งพลังงานอย่างง่ายได้ด้วยตัวเอง ในการทำเช่นนั้น คุณจะต้องเตรียมอุปกรณ์ดังต่อไปนี้:
- ถ้วยพลาสติก
- อิเล็กโทรไลต์ ซึ่งอาจเป็นสารละลายเกลือ โซดา หรือกรดซิตริกเจือจางในน้ำ
- แผ่นโลหะสองชนิดที่แตกต่างกัน ตัวอย่างเช่น อะลูมิเนียมและทองแดง
- สายไฟ
กระบวนการผลิต
นำถ้วยพลาสติกมาเทสารละลายอิเล็กโทรไลต์ลงไป อย่าเทจนเต็มถ้วย ควรเว้นช่องว่างไว้ประมาณ 1-2 เซนติเมตร ต่อสายไฟเข้ากับแผ่นโลหะ จากนั้นวางแผ่นทองแดงและแผ่นอลูมิเนียมไว้ที่ขอบของภาชนะ โดยให้ขนานกัน เมื่อทุกอย่างพร้อมแล้ว คุณสามารถวัดแรงดันไฟฟ้าด้วยโวลต์มิเตอร์ได้
เชื่อมต่ออุปกรณ์และนำหัววัดไปแตะกับขั้วของแหล่งจ่ายไฟ กดค้างไว้จนกว่าหน้าจอจะแสดงค่าแรงดันไฟฟ้า โดยทั่วไปจะอยู่ที่ 0.5-0.7 โวลต์ ค่าเหล่านี้ขึ้นอยู่กับอิเล็กโทรไลต์ หรือที่แม่นยำกว่านั้นคือ สารที่ใช้เป็นอิเล็กโทรไลต์
นี่คือวิธีการสร้างเซลล์ไฟฟ้าเคมีแบบทำเองที่บ้าน